配位子が堆積したイオンチャネルは、で開きます。 イオンチャネル。 予定。 分子構造。 選択フィルター。 イオンチャネルを介したイオン輸送のメカニズム。 リガンド沈着カルシウムチャネル
12.イオンチャネル...
イオンチャネルは十分位数のサブユニットで構成されており、イオンチャネル内のそれらの数は3から12サブユニットになります。 サブユニットの構成については、それがチャネルに入るときに、(同じタイプの)相同である可能性があり、いくつかのチャネルが異なるタイプのサブユニットによって形成される。
サブユニットの皮膚は、膜貫通セグメント(非極性部分、α-ヘリックスでねじれている)、内部クリチナルループおよび末端ドメイン(分子の極性領域によって表され、それを超えて突出するドメインを形成する)のデカール(3つ以上)で構成されています膜間球)。
膜貫通セグメントからの皮膚、内部のクリチナルループの姿勢、およびドメインの末端靭帯は、その機能から逸脱しています。
したがって、膜貫通セグメント2は、チャネルの選択性を決定するα-ヘリックスとして編成されます。
ドメインの最後のセグメントは、ポストおよび細胞内リガンドに対するセンサーとして機能し、膜貫通セグメントの1つは電位沈着センサーの役割を果たします。
サブユニットの3番目の膜貫通セグメントは、門脈管システムの操作にとって2番目に重要です。
Інніチャネルは、促進拡散のメカニズムの背後で機能します。 それらのRukhは、チャネルが同じ濃度勾配でアクティブ化されたときのイオンです。 膜を通過する移動速度は毎秒10イオンになります。
特異性 イオンチャネル.
それらの多くは、selective、tobtoに設定されます。 1種類のイオン(ナトリウムチャネル、カリウムチャネル、カルシウムチャネル、陰イオンチャネル)のみを通過させるチャネル。
チャネル選択性。
チャネルの選択性は、振動フィルターの存在に依存します。
この役割は、チャネルのコブピットによって果たされます。これは、最も強力な電荷である構成と拡張(直径)であり、歌うタイプのイオンのみをチャネルに通過させることができます。
イオンチャネルからの作用は非選択的であり、例えば、ターンのチャネルである。 したがって、細胞からの濃度勾配に沿って穏やかな状態にある膜のチャネルは、K +イオンに入り、これらのチャネルを通って、濃度勾配に沿って穏やかな状態のクリチンに侵入し、少数のNa+に入る。イオン。
イオンチャネルセンサー。
イオンチャネルのセンサーは、信号を受信するため、チャネルの敏感な部分であり、その性質は異なる場合があります。
これに基づいて、彼らは見ます:
電位沈着イオンチャネル;
受容体イオンチャネル;
リガンドケレーション(リガンド沈着);
mechanokerovanie(メカノデポジット)。
センサーを構成するチャネルはカーネルと呼ばれます。 一部のチャネルには外部センサーがあります。 このようなチャネルは非硬化と呼ばれます。
イオンチャネルへのゲートウェイ。
チャンネルはゲートであり、信号の流入で穏やかなキャンプとvіdkrivayutsyaでyakіが閉じました。 これらのチャネルでは、アクティブ化(mゲート)と非アクティブ化(hゲート)の2種類のゲートが見られます。
イオンチャネルの3つの段階を見ることができます:
ゲートが閉じていて、イオンがチャネルにアクセスできない場合、私は落ち着きます。
ポータルシステムがベントされ、チャネルに沿って膜を通って移動する場合、アクティベーションステーション。
チャネルが閉じて刺激に反応すると、非アクティブになります。
Shvidk_stが実施しました(提供者)。
スウェーデンと通常のチャンネルがあります。 「vіdplivu内の」チャネル-povіlnі、ニューロン内のナトリウムチャネル-shvidki。
膜には、それがクリチンであるかどうかにかかわらず、クリチンの機能的な陣営を沈着させる活性化の形で、さまざまな(スウェーデン性のための)イオンチャネルの素晴らしいセットがあります。
潜在的なチャネル。
潜在化チャネルは次のもので構成されます。
選択フィルター;
活性化および不活性化ゲート;
電圧センサー。
水で満たされたポリ;
チャネルの直径はイオンの直径よりも大幅に大きく、選択フィルターのゾーンでは、ワインは原子膨張まで鳴ります。したがって、チャネルに選択フィルターの機能を与えることは安全です。
Vіdkrittjaは、comironメカニズムの閉鎖は、膜電位の変化のせいであり、さらに、ゲートは、膜電位の1つの値で開き、異なるレベルの膜電位で閉じます。
膜の電界の変化は、電圧センサーの名前をとったチャネルの壁にある特別なスペーサーによって受け取られることが重要です。
膜電位の変化に拘束され、チャネルを形成するタンパク質分子のコンフォメーションを呼び出し、最後の手段として、イオンチャネルの破壊または閉鎖につながる私の位置の変化。
チャネル(ナトリウム、カルシウム、カリウム)は、相同ドメイン(サブユニット(I、II、III、IV))を持つ場合があります。 ドメイン(ナトリウムチャネルのお尻から)は、a-ヘリックスのように組織化された6つの膜貫通セグメントで構成されており、スキンがその役割を果たします。
したがって、膜貫通セグメント5は細孔の役割を果たし、膜貫通セグメント4は、膜の電位の変化に反応するセンサーであり、他の膜貫通セグメントは、チャネルへのポータルシステムの活性化および不活性化に関与する。 最後まで、他の膜貫通セグメントとサブユニットの役割は知られていません。
ナトリウムチャネル(内径0.55 nm)は、覚醒している組織の細胞に見られます。 異なる組織の1ミクロン2あたりの幅は同じではありません。
したがって、ニメリン神経線維には50〜200の管があり、ミエリン神経線維(ランビの重なり)には1ミクロン2の膜面積あたり13,000があります。 静かな悪臭を閉じてください。 膜の貯蔵電位は70-80mVです。
podraznikの注入は、膜電位を変化させ、電位沈着ナトリウムチャネルを活性化します。
Vinは、膜電位が高く、脱分極の臨界レベル近くの静止電位に等しいときに活性化されます。
強力なナトリウムストラムは、膜電位を臨界レベルの脱分極(CUD)に固定します。
膜電位を-50〜40 mV、tobtoに変更します。 脱分極の臨界レベルのレベルまで、他の電位沈着N +チャネルの閾値を上げ、それを通して入力ナトリウムストラムが放出され、それが二電位の「ピーク」を形成する。
それらは、濃度勾配とチャネルを通る化学的勾配がクリチナに移動した後にナトリウムを生成し、いわゆる流入ナトリウムストラムを形成します。これは、脱分極プロセスのはるかにスウェーデン的な発展につながります。
膜電位は、距離の符号を+ 10〜20mV変化させます。 正の膜電位は、ナトリウムチャネルの閉鎖、それらの不活性化につながります。
ポテンシャルに依存するN+チャネルは、di、tobtoのポテンシャルを形作る上で役割を果たします。 クライアントで目覚めるプロセス。
それらは、潜在的に沈着したナトリウムチャネルにカルシウムを追加し、応答パラメーターを変更します。
前 + -チャネル
カリウムチャネル(内径0.30 nm)-細胞質膜では、細胞からカリウムを「注入」するかなりの数のチャネルが明らかになりました。
落ち着いた悪臭を放ちます。 それらを通して、細胞からのカリウムの「ビティック」は、濃度勾配と電気化学的勾配の後ろのステーションで落ち着きます。
このプロセスは、カリウムストラムの放出として示され、穏やかな膜電位(-70-80 mV)の形成につながります。 気カリウムチャネルは、精神的に潜在的な沈着物にのみもたらすことができます。
膜電位の変化に伴い、脱分極のプロセスはカリウムストローマを不活性化します。
再分極の間に、入ってくるK +ストラムが電位沈着チャネルを介して形成され、これは、より線状の直線化のK +ストラムの名前をとって形成される。
別のタイプの潜在的に堆積されたK+チャネル。 それらの後ろには、膜電位(正の微量電位)の閾値下領域に出てくる強いカリウムストラムがあります。 チャネルの不活性化は、微量の過分極によるものです。
電位沈着カリウムチャネルの2番目のタイプは、通常は不活性化される一過性カリウムストラムの形で、前方過分極後にのみ活性化されます。
それらは、潜在的に沈着したカリウムチャネルのカルシウムを解放し、応答のパラメーターを変化させます。
Sa + -チャネル。
潜在的アルケレーションチャネルは、細胞質へのカルシウム流入の調節と電気発生の両方でこの入力を改善します。
カルシウムチャネルを調節するタンパク質は、5つのサブユニット(al、a2、b、g、d)で構成されています。
alformujeのメインサブユニットは、カルシウムチャネルのさまざまなモジュレーターの上部チャネルと通信の場所です。
カルシウムチャネルの構造的に異なるアルサブユニットが、ssavtsの神経細胞(A、B、C、Di Eと名付けられた)で発見されました。
機能的にカルシウムチャネル 他の種類 1つの活性化の1つのタイプ、動力学、単一チャネルの伝導、および薬理学が考慮されます。
クリチンでは、最大6種類の増強カルシウムチャネルが報告されています(T-、L-、N-、P-、Q-、R-チャネル)。
潜在的なアルケリングプラズマチャネルの活性は、さまざまな内部細胞セカンドメッセンジャーおよび膜被覆Gタンパク質によって調節されています。
カルシウム電位沈着チャネルは、ニューロンの多数の細胞質膜、滑らかで横方向に皺のある心臓の悪性腫瘍の筋細胞、および小胞体の膜に見られます。
SPRのCa2+チャネルは、SPR膜に注入されたオリゴマータンパク質です。
Sa 2+ --cerovanie Sa 2+ -SPRチャネル。
カルシウムチャネルは、以前は骨格および心臓の悪性腫瘍から見られていました。
これらの粘膜組織におけるSPRのCa2+チャネルは、異なる遺伝子によってコードされている可能性があることが判明しました。
心臓病におけるSPRのCa2+チャネルは、カルシウム結合タンパク質を介して原形質膜(L型)の高閾値Ca 2+チャネルと直接接続されており、それによって機能的に活性な構造である「トライアド」を確立します。
骨格組織では、原形質膜の脱分極は、小胞体のCa 2+シグナル伝達を直接活性化します。これは、原形質膜のCa 2+チャネルが、活性化シグナルの間接的なCa2+チャネルへの電位感受性伝達として機能するためです。タンパク質の結合によるSPR。
このように、Ca 2+-骨格筋のデポーは、脱分極(RyR1型)をもたらすCa2+放出のメカニズムである可能性があります。
骨格潰瘍の観点から、心筋細胞の小胞体Ca 2+チャネルは原形質膜と関連しておらず、デポーからのCa 2+の刺激には、細胞質ゾルカルシウム(RyR2型)の濃度を増加させる必要があります。
Krym tsikh2種類のCa2+活性化Ca2hチャネル、少し前に、3番目のタイプのCa 2+チャネルSPR(RyR3タイプ)が特定されましたが、これでは不十分です。
すべてのカルシウムチャネルは、ナトリウムチャネルとともに共通の活性化および共通の不活性化によって特徴付けられます。
粘膜細胞の脱分極(細胞質膜のビピネーション-T-細管は小胞体の膜に達する)により、筋小胞体の膜にカルシウムチャネルが沈着する可能性があります。
Oskilkiは、一方ではSPRのカルシウム濃度が高く(カルシウムデポー)、細胞質のカルシウム濃度は低いですが、他方では、SPRの膜面積とカルシウムのギャップそれらのチャネルは大きく、細胞質のカルシウムレベルは100倍に増加します。
カルシウムの濃度を上げて、急速な筋原線維のプロセスを開始します。
心筋細胞のカルシウムチャネルは細胞質膜に位置し、L型カルシウムチャネルに横たわっています。
+ 20〜40 mVの膜電位で活性化され、入力カルシウムストラムを形成します。 それらは活性化されたステーションに長期間留まり、心筋細胞の可能性のための「プラトー」を形成します。
陰イオンチャネル。
細胞膜の塩素のチャネルの最大数。 細胞は細胞間otochennyamに対してより少ない塩化物イオンを持っています。 したがって、チャネルが開いている場合、塩素は濃度勾配と電気化学的勾配の背後にあるクリチンに流入します。
HCO 3のチャネル数はそれほど多くはなく、チャネルを介した陰イオンの輸送には少なくなります。
Інні交換器。
膜には、イオンの拡散を促進するイオン交換体(キャリアタンパク質)があります。 濃度勾配に沿って生体膜を通過するイオンの移動が加速されるため、プロセスはATPに依存しません。
Na + -H +、K + -H +、Ca 2+ -H +交換体、および陽イオンを陰イオン(Na + -Ca 2+)に、または陰イオンを陰イオン(Na + -Ca 2+)に交換する交換体の最大の種類。 Cl-HCO3)。
受容体イオンチャネル。
Lgandkerovanі(ligandzalezhnі)イオンチャネル。
コアイオンチャネルのリガンドは、コアチャネルの受容体のサブタイプであり、生物学的に活性な発話(BAS)の受容体に依存しています。
見られる運河の受容体は、イオノトロピック型の膜受容体であると考えられており、生物学的に活性な物質(リガンド)と相互作用すると、急速な反応を引き起こします。
イオンチャネルのリガンド結合は、以下で構成されています。
水で満たされたポリ;
選択フィルター;
アクティベーションゲート;
リガンド結合中心(受容体)。 非常にエネルギー的にアクティブなBASVolodyahigh
同じタイプの受容体への胞子(親和性)。 イオンチャネルが活性化されると、イオンイオンは濃度勾配と電気化学的勾配の背後に移動します。
膜受容体では、リガンド結合中心は、膜の外面からリガンドにアクセス可能である可能性がある。
ホルモンとパラホルモン、イオンはこのようにリガンドとして作用します。
したがって、N-コリン作動性受容体の活性化のために、ナトリウムチャネルが活性化される。
カルシウムの浸透は、ニューロンのアセチルコリン、グルタミン酸(NMDAおよびAMPA /カイナトタイプ)受容体、およびプリノ受容体によって開始されます。
GABA A受容体はイオン性クロライドチャネルに結合し、クロライドチャネルとグリシン受容体に結合します。
膜受容体では、リガンド結合中心は、膜の内面からリガンドにアクセス可能である可能性がある。
この場合、他の仲介者、または他の仲介者自体によって活性化されるプロテインキナーゼがリガンドとして機能します。
したがって、プロテインキナーゼA、C、G、カチオンチャネルのリン酸化タンパク質は、それらの浸透を変化させます。
メカノセロン化イオンチャネル。
Mechanokerovanieイオンチャネルは、ビリピッドボールの気密性を変更するか、クリチン細胞骨格を介して、イオンの導電率を変更します。 非人格的な機械化された運河は機械受容器に接続されており、悪臭は聴覚細胞、泥紡錘体、および血管内皮に見られます。
すべての機械的にカーニングされたチャネルは、2つのグループに分けられます。
伸ばされたクリチン(SAC)のときに活性化されます。
伸ばされたクリチン(SIC)のときに不活性化されます。
メカノセラミック運河には、すべての主要な運河標識があります。
それは水で満たされる時です。
商業的メカニズム;
引っ張りに反応するセンサー。
新しいチャネルをアクティブにすると、イオンは濃度勾配に沿って移動します。
ナトリウム、カリウムATPアーゼ。
ナトリウム、カリウムATPase(ナトリウム-カリウムポンプ、ナトリウム-カリウムポンプ)。
これは、2つのαサブユニットと2つのβサブユニットの4つの膜貫通ドメインで構成されています。 αサブユニットは大きなドメインであり、βサブユニットは小さなドメインです。 イオン輸送の結果として、大きなサブユニットがリン酸化され、イオンがそれらの間で移動します。
ナトリウム、カリウムATPaseは、細胞内培地でナトリウムとカリウムの恒常性を維持する上で最も重要な役割を果たします。
気候の高いrіvenK+と低いrіvenNa+をサポートします。
電位diの生成において、膜電位の穏やかな形成に参加します。
膜を介したより有機的なスピーチの輸送を保証します(二次能動輸送)。
H2Oの恒常性に関するsuttvovplyvaetsya。
内部空間の姿勢でのイオン非対称性の形成において最も重要な沈着物を奪うためのナトリウム、カリバATPアーゼ。
ナトリウムの段階的な作業、カリウムポンプは、膜を介したカリウムとナトリウムの非等価な交換を保証します。
Sa + -ATPase(ポンプ)。
細胞質からのCa2+イオンの吸収に最も効果的なCa2+ポンプには、原形質膜のCa2+ポンプと小胞体のCa2+ポンプの2つのファミリーがあります。
たんぱく質の1つのファミリー(いわゆるATPアーゼのPクラス)まで匂いを嗅ぎたいので、これらのポンプは体内での活動、機能的活動、および薬理学を示します。
多数の細胞質膜で発生します。 穏やかな細胞の細胞質では、カルシウムの濃度は10-7 mol / lである必要があり、細胞の位置は-10-3 mol/lと大幅に高くなっています。
濃度のこのような有意差は、細胞質Ca++-ATPaseの働きを考慮に入れています。
Ca 2+プラズマポンプの活性は、中間のCa 2+なしで制御されます:細胞質ゾル中の遊離カルシウムの濃度の増加は、Ca2+ポンプを活性化します。
カルシウムイオンチャネルを介した穏やかな拡散では、それが不可能な場合があります。
Ca-ATPaseは、Caを細胞から反対の濃度勾配の細胞内中央に輸送します。 Ca +勾配によると、イオンチャネルを介したクリチンの拡散の兆候があります。
小胞体の膜にも大量のCa++-ATPaseが含まれています。
小胞体カルシウムポンプ(SERCA)は、カルシウムを細胞質ゾルから小胞体に輸送します。これは、一次能動輸送のためのカルシウムの貯蔵庫です。
デポでは、カルシウムはカルシウム結合タンパク質(カルセクエストリン、カルレティキュリンなど)と結合します。
この時間では、SERCAポンプの3つの異なるアイソフォームが説明されました。
SERCA1サブタイプは柔らかい骨格組織専用であり、SERCA2ポンプは他の組織で広く拡張されています。 SERCA3ポンプの重要性はあまり明確ではありません。
タンパク質SERCA2-nacocіvは、心筋細胞と平滑筋に特徴的なSERCA2aと脳組織に特徴的なSERCA2bの2つの異なるアイソフォームに細分されます。
細胞質ゾル中のCa2+の増加は、小胞体へのカルシウムイオンの摂取を活性化し、小胞体の中央での遊離カルシウムの増加は、SERCAポンプを活性化します。
H + K + -ATPase(ポンプ)。
ダクトの粘膜の壁側(壁側)細胞におけるこのポンプの助けのために(1つのATP分子の加水分解の結果として)、後部空間からクリーチンへの2つのカリウムイオンとH+の2つのイオンの輸送後腔の細胞質ゾルから発生します。 このメカニズムは、スラグ中の塩酸の溶液に基づいています。
イオンポンプクラスF.
ミトコンドリアATPアーゼ。 ATP合成の最終ステップを触媒します。 ミトコンドリアの陰窩はATP合成酵素を攻撃します。ATP合成酵素はクレブス回路で酸化され、ADPがATPにリン酸化されます。
イオンポンプクラスV.
リソソームH+-ATPase(リソソームプロトンポンプ)–細胞質ゾルから一連のリソソームオルガネラ、ゴルジ装置、分泌小胞へのH+の輸送を確実にするプロトンポンプ。 その結果、たとえばリソソームではpH値が5.0に低下し、これらの構造の活性が最適化されます。
イオン輸送の特徴
1.重要で非対称の膜貫通! 穏やかな場合はNa+とK+の勾配。
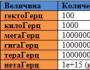
クリチン(145ミリモル/ l)のナトリウム姿勢は10倍高く、クリチン(14ミリモル/ l)では低かった。
クリチン(140ミリモル/ l)中のカリウムはクリチン(4ミリモル/ l)よりも約30倍高いです。
Tsyaosoblivіstrozpodіlіonіvnatіyuikalіyu:
Na + / K+-nacocaロボットによってホメオスタットされました。
穏やかな出口カリウムストラム(ターンチャネル)で形成します。
平和の可能性を形成します。
カリウムチャネル(電位沈着、カルシウム沈着、リガンド沈着)の働きは、腹側カリウムストリームの形成に向けられています。
これは、膜を腹側レベルに変える(再分極段階中の電位沈着チャネルの活性化)か、または膜を過分極化する(他のメディエーターのシステムによる活性化を含む、カルシウム沈着、リガンド沈着チャネル)。
後流で母親をフォローしてください、sho:
膜zdijsnyuetsyaパス受動輸送を介してperemishchennyaカリウム;
zbudzhennya(潜在的なdії)を形作るzavzhdiozumovlenvhіdnimnatriєvimstrum;
任意のナトリウムチャネルの活性化、入力ナトリウムストラムを絶えず活性化する;
受動輸送の膜zdіysnyuєtsyamayzhezavzhdi経路を通るperem_shchennyaナトリウム;
エピカルクリチンでは、スティンカリズニッチチューブの組織、ゴロズニン(小腸、カナルツヤネフロンTA)、キルキスティカナリフ、ストリミのアクティバ、バザエリストラップの呼び出し、およびバザエルの基部で強引に。細胞からナトリウムを送り出すカリウムポンプ。 ナトリウム輸送システムのそのような非対称的な分布は、ナトリウムの経細胞性、tobtoの伝達を確実にします。 腸の内腔から、体の内側中央にあるニルク細管。
電気化学的勾配によるナトリウムのクリチンへの受動輸送は、豊かな音声の二次能動輸送に勝つ方法として、エネルギーの蓄積につながりました。
2.細胞の細胞質ゾル中の低レベルのカルシウム。
穏やかな場合は、カルシウム(50 nmol / l)の代わりに、患者の低い位置(2.5 mmol / l)で5000分の1になります。
細胞質ゾル中のそのような低レベルのカルシウムは非暴力的であり、濃度のカルシウム破片は、信号の実装における別の内部クリチンメディエーターのように、外側の隆起よりも10〜100倍大きい。
そのような心の中で、小胞体(小胞体-カルシウムの「デポー」細胞)。
チャネルの開放によって支援されるカルシウムの流れの形成は、細胞質ゾル中のカルシウムの濃度の生理学的に有意な増加を確実にする。
細胞の細胞質ゾル中の低レベルのカルシウムは、Ca2 + -ATPase、Na + / Ca2 +交換体、細胞質ゾルへのカルシウム結合タンパク質によって刺激されます。
細胞質ゾルCa2+と細胞質ゾルCa2+結合タンパク質、細胞質ゾルを消費するカルシウムイオンとの高速結合のクロムは、ゴルジ装置またはミトコンドリアのCa2+デポーによって閉塞された細胞核によって蓄積することができます。
3.クリチン中の低レベルの塩素。
塩素(8 mmol / l)の存在下で穏やかな場合は、10分の1になります。
このようなミルは、K +/Cl-コンベヤーロボットによってサポートされています。
クリチンの機能状態の変化は、塩素に対する膜透過性の変化に結びついています(または結合しています)。 プロトン性およびリガンド硬化性クロライドチャネルの活性化により、イオンは受動輸送の経路を通ってチャネルを通ってサイトゾルに入ります。
さらに、サイトゾルへの塩素の侵入は、Na + / K +/2CH共輸送体とCG-HCO3交換体の側で形成されます。
クリチンに塩素が入ると、膜の極性が過分極になります。
イオン輸送の特徴は、情報をエンコードし、構造の機能ステーションを指定し、ある機能状態から別の機能状態に移行するため、臓器や組織で生体電気現象を形成する主な役割を果たします。
イオンチャネルは内在性タンパク質であり、濃度勾配の背後でイオンの受動輸送を保証します。 輸送のためのエネルギーは、膜の両側のイオン濃度の差です(膜貫通イオン勾配)。
非選択チャネルは非常に強力な場合があります。
・すべてのタイプのイオンを通過させますが、イオンK +の浸透は大幅に高く、他のイオンの浸透は低くなります。
- 常にvіdkritustanіで知っています。
選択チャネルは非常に強力です。
・1種類のイオンのみを通過させます。 皮膚タイプのイオンの場合-独自のタイプの運河;
- クローズ、アクティブ、非アクティブの3つの状態のいずれかになります。
選択チャネルのViborcha浸透が確保されます 選択フィルター、負に帯電した原子からのリングのある種の肯定は、最高のミストチャネルで見られるように、酸っぱいです。
チャネルの変更は、ロボットゲートメカニズムによって保護されます , これは2つのタンパク質分子によって表されます。 タンパク質分子の数、sov。 活性化ゲートと開始ゲートは、それらのコンフォメーションを変更すると、イオンチャネルを歪める可能性があります。
ステーションでは、アクティベーションゲートが閉じられ、不活性化ゲートが閉じられます(チャネルが閉じられます)(図2.3)。 ゲートがシステムに送られると、活性化ゲートが開き、チャネル(活性化チャネル)を介したイオンの輸送が開始されます。 細胞膜の著しい脱分極により、不活化ゲートが閉じ、イオンの輸送が接続されます(不活化チャネル)。 MPのレベルを変更すると、チャネルは出口(閉鎖)ステーションで曲がります。
活性化ゲートを呼び出す信号に応じて、選択的イオンチャネルは次のように細分化されます。
化学感受性チャネル-活性化ゲートを開き、新しいリガンドに付着した結果としてチャネルに関連する受容体タンパク質のコンフォメーションを変化させるシグナルとして。
- 潜在的な敏感なチャネル-活性化ゲートへの信号-脱分極の臨界レベル(CUD)と呼ばれるレベルまでのクリチン膜のMP(脱分極)の減少。
アクティベーション方法の背後にあるものを見ることができます:
· 潜在的に活性化 イオンチャネル(出口段階で閉じた状態から戻る遷移は、膜電位が変化したときのタンパク質分子のコンフォメーションの影響を受けます)。 バットは潜在的な沈着ナトリウムチャネルである可能性があり、これは潜在的なdiyの生成中の細胞の脱分極を意味します。
· 機械的に敏感 イオンチャネル(皮膚の機械受容器の活性化など、機械的刺激がクリチン膜に注入されると開きます)。
· リガンド活性化 Інніチャネル。 悪臭を活性化する方法によれば、それは、リガンドが膜のどちら側に注がれるかに応じて、2つのグループ(エクストラクリチンおよび内部クリチン)に細分される。 神経筋シナプスにおける覚醒のシナプス伝達の場合の刺激(例えば、アセチルコリン)として( このお尻イオンチャネルの十分位数タンパク質サブユニットの1つであるコリン作動性受容体)は、粘膜細胞の膜の外面に広がり、イオンチャネルを開き、陽イオンを透過します。 リガンド活性化チャネルはクリチンの二次中間体にありますが、静脈内のそれらの遷移は、細胞質内の特異イオンの濃度の変化に依存するようになります。 バットは、細胞内のカルシウムイオンの濃度の増加とともに活性化されるカルシウム活性化カリウムチャネルである可能性があります。 このようなチャネルは、作用の可能性が完了した後、膜の再分極に関与します。
膜電位、等イオン電位、静穏電位について理解する。 洗って、平和の既存の汗を引き起こします。 等しい投稿フィールド。Funktsmembptentsialu。
平和の可能性のためにその理由を洗ってください。
研究者と実験データは、「運用上の」平和の段階にある体内のすべての細胞が単一の程度の分極によって特徴付けられることを証明しています。 皮膚細胞のプラスモレンマは帯電しており、穏やかな内面は負の細胞間培地電位を持っています。 異なる細胞の膜電位差は異なりますが、どこでも数十ミリボルトに達します。 微小電極技術の助けを借りて、クリチン膜の両側の電位の実際の差を直接測定する実験を行いました。
イオンチャネルとイオンチャネルはどのようにして生体電気発生を保証しますか? これまで、落ち着きの可能性とDIYの可能性への主な貢献は、chotiriioniに貢献することであることは明らかです。 Na + K + Ca ++ Cl-呼吸イオンチャネルを介して歌う心の通常の浸透(または浸透ではない)。
最初のイオン(maє電荷)が膜を透過できるようにするには、次のことを理解する必要があります。
1.濃度勾配の外観(イオンポンプのロボットによって作成された)
2.電気化学的勾配の存在(荷電粒子の濃度と、膜の両側から陽イオンと陰イオンを分離するイオンチャネルの力の合計によって作成されます)。
3.Nyavn_st v_dpov_dnykhkanal_v_v_dkritomstan_。
で 落ち着く可能性クリチン膜の内側が帯電している可能性があり、その兆候(陰性)が示されています 有機アニオンの細胞質における存在(bіlkіvとアミノ酸)、イオンチャネルを透過することができません、そして プローションの不足-カリウム陽イオン、カリウムイオンチャネルを透過することができ、その結果、細胞は過剰な負イオンを持ち、隙間-過剰な正電荷を持ちます。 クリチンの負電荷と細胞間空間の正電荷の大きさは数学的に与えられますが、単純なモード、たとえば巨大なイカの軸索に対してのみです。
静けさの可能性の拡大は、ホジキン、ゴールドマン、カッツによって提唱された安定したフィールドの近接性の観点から説明されています。
Vm \ u003d RT / zFln((pko + pNa o + pCl i) / (pki + pNa i + pCl i))
誤解の痕跡ではありません 膜電位, 等しいポテンシャルі 落ち着く可能性.
膜電位は、イオンチャネルを透過できる電荷の合計によって決定されます。
等しい電位は、細胞の原形質膜のそのような電位であり、膜を通るそのような総ストラムイオンは、直接であるそのようなイオンと引き換えに水チャネルを貫通する10個のイオンの能力に関係なく、ゼロに達する。増殖性のものから直接。 ネルンストの等式で表されます。
静止膜電位の機能:
1.目覚めと亜鉛メッキを念頭に置いた膜の分極。
2.分極は、シナプス前終末からメディエーターの視力を決定します。
3. PPは、閉じた鋼の潜在的な堆積チャネルを認識するための頭脳を作成します(膜の分極は、DIYの可能性を形成するための頭脳を作成します)。
神経系の生理学
神経中枢の概念。
神経中枢-中枢神経系の構造の構造は、体の他の機能の安全な調節の活動、または反射作用によって調整されます。 神経中枢の構造的および機能的基礎に関する記述は、中枢神経系における機能の局在化に関する理論の発展の歴史に基づいています。 神経中枢の力:
2.中枢神経系のニューロンのうっ血の伝導の改善。 1つの細胞間接触のシナプスzatrimkaTsynは、約0.5〜2ミリ秒です。 細胞内にはn個のニューロンがありますが、脳への信号の総潜伏期間はn×T synであり、さらに重要である可能性があります。 ちなみに、中枢神経系の信号の時間(反射の合計時間と神経ストーバーの伝導に費やされた時間の改善から計算)を知ることで、シナプス遷移の数を推定することができます(n )特定の反射の線量で。
4.覚醒の片側伝導、およびシナプス入力の発散と収束は、閉じたニューロンの槍からの覚醒(残響)の循環のための形態学的基質を作成します。 この症状が短時間の記憶の基礎であることが重要です。
5.核に関連するニューロンを歌うために、それは特徴的です バックグラウンドアクティビティ。 それは膜の力に依存し、自発的な脱分極の形で横たわっています。 他のニューロンは「動いて」おり、シナプス入力がアクティブ化されたときにのみAPを生成します。
6.ニューロンとその表面シナプスに見られるニューロンの場合、酒に見られるさまざまな発話、シグナル伝達分子、代謝物に対する感受性が特徴的です。
7.胃は特徴的であり、これの理由の1つは、明確なメディエーターの予備の変化と合成の低速です。
8.可塑性。 緩和、効力(強縮後の強縮、長期にわたる)うつ病は、受容体の優勢、その後のプロセス、およびニューロンの表面上の新しいシナプス接触または受容体の出現によって示されます。
脳の神経索は、片側がまっすぐになっているのが特徴です。 (線形)ウェイクアップコール。 Якщо є ланцюжок нейронів, пов'язаних між собою синаптичними контактами, то через властивість хімічних синапсів виділяти медіатор із пресинаптичного закінчення в синаптичну щілину і рецептувати його рецептором, локалізованим на постсинаптичній мембрані, вектор поширення збудження в нейронній мережі спрямований у бік наступного постсинаптического нейрона. 熱いお尻で 与えられた原則є法 ベラ-マジェンディ(求心性線維は背側から脊髄に入り、ルホビ線維は前根から脊髄を満たします)。
プロセス 収束それらは、デカール神経細胞から1つの同じニューロンへのさまざまなインパルスフローの収束で発生します(div。4.1.4)。 収束のプロセスは、同じタイプの神経細胞に典型的です。 たとえば、脊髄の運動ニューロンでは、一次求心性線維のクリムが、脊髄上および脊髄上部の中心、ならびに中間ニューロンの興奮性およびガルミカルな挿入において、さまざまな下部管の線維を収束させます。 その結果、脊髄の運動ニューロンは、脳の超分節装置を含む数値神経構造の中央末端経路の機能を発達させ、これがルホボイ機能の調節につながる可能性があります。
発散神経細胞の構築は、ウクライナとさまざまな神経細胞との数値的なシナプス接続を確立するために呼び出されます。 このため、1つの神経クリチナがさまざまな反応に関与し、他の多数のニューロンの興奮を伝達して破壊する可能性があります。 多数ニューロン、中枢神経系の覚醒過程の広い照射を確実にします。
ブドフニューロン。
機能的には、脊髄ニューロンは4つの主要なグループに分けることができます。
1)運動ニューロン、またはrukhovi、-前角の細胞、その軸索は前根を形成します。
2)介在ニューロン-脊髄神経節から情報を受け取り、後根に位置するニューロン。 Qiニューロンは、痛み、体温、触覚、振動、固有受容性のからかいに反応します。
3)交感神経、副交感神経ニューロンは、甲虫の角でより重要に発達します。 これらのニューロンの軸索は、前根の倉庫の脊髄から出現します。
4))結合細胞-脊髄の上部装置のニューロンであり、中央およびセグメント間にリンクを確立します。
運動ニューロン。 運動ニューロンの軸索とその末端は数百のm'yazovyh線維であり、運動ニューロンユニットを確立します。
介在ニューロン。 1秒あたり最大1000の頻度でインパルスを生成する中間ニューロンはバックグラウンドアクティブであり、樹状突起に最大500のシナプスを持つことができます。 介在ニューロンの機能は、脊髄の構造間の接続の組織化、および脊髄のクリチナムおよび他のセグメントへの上部および下部チャネルの提供に関与しています。 介在ニューロンのもう1つの重要な機能は、ニューロンの活動を活性化することです。これにより、目覚めの直接的な経路が確実に維持されます。
自律システムの交感神経モデルのニューロン。 脊髄の胸部の角にあるRostashovani。 ニューロンの数はバックグラウンドアクティブですが、通常のインパルス周波数(1秒あたり3〜5)もあります。
自律システムの副交感神経枝のニューロン。 それらは脊髄の仙骨部分の近くに局在し、バックグラウンドアクティブです。
ニューログリア、またはグリアは、神経組織の細胞要素のコレクションであり、さまざまな形状の特殊な細胞で構成されています。 グリア細胞はニューロン間の空間を覆い、脳の40%を占めています。 グリア細胞ローズマリーの後、3〜4倍少なく、神経質になります。 世紀の間に、人間の脳のニューロンの数は変化し、グリア細胞の数は増加します。 分類:
楕円形の核と少量のクロマチンを持つ豊富な増殖性クリチンを持つ星状細胞。 アストロサイトのサイズは7〜25ミクロンです。 roztashovuyutsyaの頭は脳の灰色のスピーチにランク付けされます。 アストロサイトの核はDNAを置き換えることができ、原形質はラメラ複合体、セントリソーム、ミトコンドリアを含むことができます。 アストロサイトはニューロンのサポートであり、神経ストーバーの修復プロセスを確実にし、神経線維を分離し、ニューロンの代謝に参加します。 アストロサイトの成長は、毛細血管を取り囲む「下部」を構成し、実際に毛細血管を曲げます。 その結果、ニューロンと毛細血管の間に星状細胞はなくなります。 たぶん、悪臭は血液からニューロンへのスピーチの輸送を確実にするでしょう。 アストロサイトは、毛細血管と上衣の間の空間を満たし、空の管を脳に織り込みます。 このようにして、アストロサイトが輸送機能を実行するように、血液と脳粘膜の脳脊髄液の故郷との間の血液の交換が確実に行われることが重要です。
オリゴデンドロサイト-少数の芽。 ローズマリー、下部星状細胞の悪臭は少なくなります。 大脳の皮質では、多くのオリゴデンドロサイトが上部のボールから下部のボールに成長します。 podkirkovyh構造、Stovbur骨髄、皮質の下部には、より多くのオリゴデンドロサイトがあります。 オリゴデンドロサイトは、mіє-nіzаtsії軸索(脳の白いスピーチに多くあります)、ニューロンの代謝、およびニューロンのトロフィーに参加します。
ミクログリアは最も豊富なグリア細胞によって表され、それはまぶしい細胞まで見ることができます。 Dzherelomミクログリアと中胚葉。 ミクログリア細胞は食作用が可能です。
14.クライアント間連絡先の現在の設定。
シナプスは接触と呼ばれ、ニューロンを自給自足として確立するために使用されます。 シナプスは折り畳み構造であり、シナプス前部(信号を伝達する軸索終末)、シナプスギャップ、シナプス後部(受容細胞の構造)で構成されています。
シナプスの分類。 シナプスは、行動の性質、信号の伝達方法に応じて分類されます。
roztashuvannyaの背後には、神経筋、シナプス、神経ニューロンがあり、軸索、軸索、軸索、樹状突起に分かれる独自のペースを維持しています。
シナプスの構造の性質の背後にある、それは刺激的で不安定である可能性があります。
信号をさらに送信するために、シナプスは電気、化学、音に分けられます。
ニューロンの相互作用の性質。 それは相互作用の方法で示されます:遠い、全体的な、接触。
離れた相互作用は、体の異なる構造に広がる2つのニューロンによって提供されます。 たとえば、神経ホルモン、神経ペプチドは脳の低構造のクリチンに確立され、それが次に他の細胞のニューロンにユーモラスさを注入します。
ニューロンの膜がより少ない細胞間空間によって分離されている場合、ニューロンの相互作用は時間とともに発達します。 ニューロンの膜とグリア細胞がない間で、そのような相互作用を鳴らしてください。 このような総和は、香りの神経の軸索、小脳の平行線維などに典型的です。相乗効果の総和が、単一の機能における血管ニューロンの運命の安全性を保証することが重要です。 ゾクレマは、ニューロンの活動の産物である代謝物が細胞間空間に注がれ、血管ニューロンに注がれる必要があります。 相互作用は、1時間の間、ニューロンからニューロンへの電気情報の伝達を確実にすることができます
医療ニュースでは、悪魔がイオンチャネルに注ぐ方法を知っている人々についての情報が絶えずあります-悪臭はそれらを活性化しようとしています、そして逆に、彼らはブロックするのを急いでいます。 たとえば、私たちは最近、イスラエルのふすまの成分に基づいて新しい無病を開発しているテルアビブ大学(テルアビブ大学)マイケルグレビッツ(マイケルグレビッツ)の教授の調査に関するレポートを公開しました黄色いサソリ-最も安全なものの1つ。 この薬は、まるで痛みを和らげる効果があるかのようにナトリウムチャネルに注射され、新世代の痛みを和らげる効果があると考えられています。 ionnіチャネルzgaduyutについて、そしてmovaが腫瘍性疾患について行く場合、heart-sudinnіvіdhilennyaとnavіtshkіdlіvіpodobannya。 では、チャネルとは何ですか?ロボットがそれほど重要なのはなぜですか?
dirkaのKlitina
クリチンは生きています-光に対して静的であり、彼らは常にスピーチの交換を持っています、クリチンと同じドブキリーとの相互作用でさえ-体の生活に必要な心のサポートです。 この交換は、イオン、アミノ酸、ヌクレオチドなどの豊富な元素の必要な浸透を消費するために、クリチンの膜(シェル)を介して、ヤクを介して実行されます。
膜が必要に応じてこれらの要素を貫通できるように、膜には特別な輸送タンパク質があり、膜に独自の「汚れ」である細孔を作ります。 直径1nm未満の水路は水分子で詰まっており、通過できる分子の種類に応じて膜チャネルを振動させることができます。 はい、たとえば、カルシウム、ナトリウム、カリウムチャネルおよび悪臭は、他のイオン、特定のクリームを許可しません。 チャネルへのそのような活気は、その電荷と構造によって組み立てられます。
それらの細孔を通るイオンの流れを実行するために、イオンチャネルは電位差をバイコリストします。 ロシアのイオンのせいであるオシルキストラムを排除することができます-さらに、単一のチャネルを誘導することが可能であり、膜イオンチャネルの挙動を追跡するのは簡単です。 チャネルは自発的に、そしてしばしばフレアアップして閉じます。 ある形式から別の形式へのIqi遷移は、X線回折、メスバウアー分光法、および核磁気共鳴によってねじれる可能性があります。 これらのチャネルは高度に組織化された構造であり、単なる水の管ではなく、崩壊している中性および荷電分子グループの迷路であることが明らかになりました。
数十種類のイオンチャネルを探索します。 最大のグループはカリウムチャネルで構成されており、最大で約40種が存在します。 私の肌の多様性は、その構造的特徴と機能が独特です。 たとえば、導電率の高いカリウムチャネル(通過するカリウムイオンが多い、チャネルが低い)は、タンパク質の丸い断片、サブユニットから形成され、α-ヘリックスに折りたたまれています。 一次らせんの深紅色も二次β構造を形成できるように、それらは明らかに短い断片を追加します。 悪臭は、それ自体で、β-1、β-2、β-3、またはβ-4に細分されます。これは、独自の力のチャネルのいくつかの皮膚です。 たとえば、β-4チャネルブロッカーはブロッカーイベリオトキシンに耐性があります。 運河の封鎖は遠く離れているので、運河を通る流れは何も通過しません。
クリチンの高組織「dirka」の必要性を新たに提起しましたか? Інніチャネルは人生の基礎です。 悪臭は、神経系の警戒心、神経から神経への神経インパルスの伝達、ホルモンの分泌を保護します。 イオンチャネルの活性化は、生理学的反応のカスケードを開始し、私たちの心にズームインし、心臓の肉とジカルダイアフラムの働きを引き起こし、私たちの好み(たとえば、アルコール)を誘発します。これらの現代は、ロボットのイオンチャネルの特性によって説明されました。
これらの重要なチャネルのブロックは、体に深刻な変化をもたらします。 イオンチャネルがその化学的攻撃の新しい痕跡の開発の主な標的になっているという事実に驚くことは何もありません。 したがって、人々に知られている最も重度の神経麻痺物質の1つは、ナトリウムチャネルを遮断するテトロドトキシンです。 テトロドトキシンは分子が大きく膨張するため、文字通りナトリウムチャネルの細孔を詰まらせ、ナトリウムイオンの通過が不可能になり、神経インパルスが細胞から細胞に伝達されなくなります。 M'yazi zavmirayut、神経系の悪臭を放つpodkoryayutsya信号さえ。 たとえば、コノトキシンに似た毒素は、ヘビや海の軟体動物の兵器庫に見られ、犠牲者を麻痺させるのに役立ちます。
医学におけるイオンチャネル
医学では 今日病気が少ないのは、ロボットのイオンチャネルの損傷によって説明されます。 喜びのさまざまな道を悪臭を放ちたいと思って、彼らの原因の一致は彼らを大きなグループで見ることを可能にしました。 悪臭には、pridbanіやspadkovіの病気のようなものが含まれます。
 2003年、イオンチャネルの構造を発見したことで、アメリカの科学者ロデリックマキノンにノーベル化学賞が授与されました。 1998年、Youmuは結晶学的手法を使用して、細菌Streptomyceslividansのカリウムチャネルのトリビミック分子構造を研究しました。 タンパク質の画像はobkladinciジャーナルScienceに掲載され、その編集者はマッキノンをロックの10の最も重要な科学的成果の1つとして尊敬していました。 このタンパク質は4つのサブユニットで構成されており、α-スパイラルバッドを形成することができます。 カリウムカチオンは中央の空の穴を通って運ばれます。 イラスト:BNL / DoE、ロックフェラー大学/ロデリックマキノン |
例えば、ナトリウムおよびカリウムを含むイオンチャネルのグループ全体の機能障害により、それらは慢性自己筋障害症候群の発症を引き起こします。 イオンチャネルの機能障害によって引き起こされる不況の病気から、ロボットのカリウムチャネルの機能不全と優れた導電性によるビクリカンのようなてんかんを推測することができます。 テキサス大学サンアントニオ校のリチャード・オルドリッチ教授によると、トランスジェニックマウスについて述べたところ、ベータ4の量が不十分なために神経の覚醒が痙攣を引き起こすKCNMB4遺伝子をブロックすることが可能でした。
β-1サブユニットの機能が不十分な場合、チャネルは高血圧の発症に関連しています。 理由としては、タンパク質β-1サブユニットのアミノ酸ウェアハウスが標準に対応していないため、そのようなサブユニットを備えたチャネルは、血管壁の拡張を刺激することができず、それを通して、動脈が引き起こされ、高血圧が発症します。 tse noteについては、たとえば、デンマーク大学(Syddansk Universitet)からのRalphKöhlerのレポート。
もう1つの広く蔓延している心血管疾患-QT延長症候群は、心臓のカリウムチャネルをコードする遺伝子の変異によって引き起こされます。これにより、カリウムチャネルの活性が高まり、心臓のカリウムの正常な流れが変化します。
カルシウムチャネルの機能が損傷すると、運動失調状態になり、混乱の調整が不可能になります。
ナレシュティ、粘膜嚢胞症(または線維嚢胞性変性症)は、塩化物チャネルをコードするCFTR遺伝子の変異による、他の原因とともに、二指腸系および粘膜腸管の重篤な疾患です。
したがって、イオンチャネルの正常な機能は、タイプに関係なく、健康な人にとって非常に重要です。
チャンネルをターゲットに!
今日、薬剤師は、まるで注射されたかのように、薬剤の製剤に積極的に取り組んでいます。 おそらく、これらの薬の中で最も人気のあるものの1つは、心拍数障害を正常化する抗不整脈薬です。 それらは、L型の主要なカルシウムチャネルを介して細胞間空間から心臓および血管の粘膜細胞へのカルシウムイオンの浸透を超越するため、「カルシウム拮抗薬」(例えば、ベラパミル)として知られています。 心臓の肉のクリチンと血管の壁のカルシウムイオンの濃度を下げると、カルシウムの拮抗作用が冠状動脈と末梢動脈を拡張します。
カリウムチャネル活性化因子(イコランジル、ミノキシジル、ジアゾキシド、ピナシジル)も、冠状血管および末梢臓器の血管の拡張を引き起こす可能性があります。 カリウムチャネルへの注射は飽和しており、脳血管のけいれんによって引き起こされる脳卒中のけいれんのために。
外科診療で人気のある麻酔薬であるリドカインとノボカインは、ナトリウムチャネルの遮断によって痛みを遮断します。 真実は、これらの準備の副作用は、悪臭が痛みと触覚の過敏症を引き起こすことです。
しかし、遠くでは、他のイオンチャネルがそのような状況で救助に来る可能性があることに注意する価値があります-いわゆる過渡受容体電位(TRP)。 このチャネルファミリーは、選択性が低く、ナトリウム、カルシウム、マグネシウムなどの正に帯電したイオンのほとんどを通過することを特徴とする不定種で利用できます。
痛みに反応する神経細胞に広がるTRP運河の特別なグループは、唐辛子の有効成分であるカプサイシンの存在に敏感です。 カプサイシンでTRPチャネルを活性化することに加えて、リドカインをさらに導入すると、わずかなTRPチャネル、つまり疼痛ニューロンでのみオンになっているチャネルのみが振動して遮断されます。 このランクでは、鎮痛剤の世話をすることができます。
ロボットチャネルのテストの容易さと、製薬業界に適した方法でそれらをテストすることの有望な結果は明らかです。 その前に、多くの基本的な準備は時間の経過とともにその効果を無駄にします:作成者が意図したように、体はそれらに聞こえ、異なる方法で反応します。 Vchenimは、postiyno shlyakhi shlyakhiusunennyaraznihzboїvとionnіkanalをもたらします。 そして、今年の彼らとの操作は、一方では何十億もの投資を獲得し、他方では、最も躁病に苦しむ人々により良い希望を与えます。
パートナーのニュース
Інніチャンネル提出物 内在性タンパク質膜。 Cіbіlkizdatnіは、歌の注入で、それが一種のイオンであろうと、それが曲がっていようと、1時間通過できるようにそれらのコンフォメーション(力の形)を変更します。 ナトリウム、カリウム、カルシウム、塩素チャネルの場合、1つのチャネルで2つのイオンを通過させることができます。たとえば、ナトリウム-カルシウムチャネルの場合です。 イオンチャネルを介して、イオンの受動輸送が少なくなります。 Tseは、水路としてイオンの移動が必要であり、イオン濃度の勾配が必要であることを意味します。 この方向では、濃度勾配に沿ってイオンの流れがあります-最高濃度の領域から最低濃度の領域へ。 私たちがイオンについて話していることを覚えておく必要があります-荷電粒子、電荷を伴うそのような電荷の輸送。 濃度勾配を1つのくちばしで真っ直ぐにすることができ、電荷が移動に強く反対している場合は、状況が可能です。
Інніチャネルは、2つの最も重要な権限である可能性があります:1) 活気 (選択性)単一イオンに対する比率と2) 丸くなることを構築(活性化)。 活性化されると、チャネルが開き、イオンを通過させます(図8)。 したがって、チャネルを形成する内在性タンパク質の複合体には、「自身の」イオンを認識する構造と、イオンの通過を認識できる構造の2つの要素が含まれます。 チャネルの選択性はこれらのタンパク質によって決定されます。承認されているため、「独自の」イオンは寸法と電荷によって区別されます。
チャネルのアクティブ化 mozhlivakіlkomshlyakhami。 まず、膜電位が変化すると、チャネルがカールしたりカールしたりする可能性があります。 電荷を変更してタンパク質分子のコンフォメーションを変更すると、チャネルがイオンに対して透過性になります。 チャネルの出力を変更するには、膜の電位にわずかな圧力を加えます。 これらのチャネルは 潜在的な預金(またはエレクトロセラミック)。 別の方法では、チャネルは、膜受容体と呼ばれる倉庫折り畳みタンパク質複合体である可能性があります。 このように、チャネルのパワーの変化は、受容体と生物学的に活性な発話(ホルモン、メディエーター)との相互作用から生じるコンフォメーションタンパク質によって結合されます。 これらのチャネルは 化学療法剤(または受容体-ケロバニ ) 。 さらに、チャネルは機械的注入中にねじれる可能性があります-逆に、伸びます(図9)。 アクティブ化を保証するメカニズムは、チャネルへのゲートと呼ばれます。 チャネルが開閉するスウェーデン性については、スウェーデンなどに分けることができます。
ほとんどのチャネル(カリウム、カルシウム、塩素)は、オープンとクローズの2か国で使用できます。 ロボットナトリウムチャネルには特定の機能があります。 カリウム、カルシウム、塩素などのこれらのチャネルは、閉じた状態または閉じた状態のいずれかで強力に中断される可能性がありますが、ナトリウムチャネルは非アクティブ化される可能性があります。図10)。
図8.固定チャネル
図9.ロボットの受容体でコーティングされた運河のバット。 ACH-アセチルコリン。 ACh分子と膜受容体との相互作用により、チャネルがイオンを通過し始めるようにゲートタンパク質のコンフォメーションが変化します。
図10バットポテンシャル-休閑チャネル
潜在的沈着ナトリウムチャネルには、活性化および不活性化ゲート(スライダー)があります。 活性化および不活性化シャッターは、異なる膜電位でコンフォメーションを変化させます。
覚醒のメカニズムを見るとき、私たちはナトリウムおよびカリウムチャネルのロボットよりも重要であり、カルシウムチャネルの特徴について簡単に言えば、悪臭は遠くにあります。 ナトリウムチャネルとカルシウムチャネルは、その優位性を求めて戦います。 ナトリウムチャネルはより一般的であり、カルシウムチャネルはあまり一般的ではありません。 ナトリウムチャネルの活性化は、LOまたはPDのいずれかの脱分極および立証にのみつながる可能性があり、カルシウムの活性化は、クリチンの代謝変化をさらに引き起こす可能性があります。 Tsіzmіniumovlenіtim、schozv'yazuєtsyazіspetіlіmiは、タンパク質に敏感です。 カルシウムタンパク質の誘導は、他のタンパク質の力の建物の変化になるように力を変化させます。たとえば、酵素を活性化し、高速のミャジブを開始します。メディエーターを参照してください。
現在の調査結果によると、生体膜はクリチンのすべての生き物の外殻を構成し、数値の内部細胞小器官を形成します。 最も特徴的な構造的特徴は、膜が常に閉じた空間を作り出すことであり、そのような膜の微細構造組織は、それらが最も重要な機能を実行することを可能にします。
Budovaと細胞膜の機能。
1.バリア機能は、追加のヘルプメカニズムを備えた膜が濃度勾配の作成に関与し、自由拡散をシフトさせるという事実によるものです。 この場合、膜は電気発生のメカニズムに関与します。 それらの前に、穏やかなポテンシャルの生成のメカニズム、薄暗いポテンシャルの生成、均質および不均質な覚醒構造の背後にある生体電気インパルスの拡大のメカニズムを見ることができます。
2.クリチン膜の調節機能は、生物学的に活性な発話の受信のための内部クリチンおよび内部クリチン反応の微調整に関与しており、これは膜の酵素系の活性の変化および発射につながる( 2番目の膜の「メカニズム」)。
3.非電気的性質の外部刺激の電気信号への変換(受容体内)。
4.シナプス終末における神経伝達物質の振動。
現代の方法 電子顕微鏡法細胞膜の数(6〜12 nm)が割り当てられました。 膜は主に脂質とタンパク質で構成されており、その数は同じではないことを示す化学分析 他の種類クリチン。 細胞膜の機能の分子メカニズムの開発の複雑さは、細胞膜が精製されているように見えるとき、それらの通常の機能が破壊されるという事実によるものです。 現時点では、最も普及しているナブラモザイクモデルの中で、クリチン膜のさまざまなタイプのモデルについて話すことができます。
モデルによれば、膜は、分子の疎水性末端が二重層の中央に位置し、親水性の方向が水相の近くにあるように配向されたリン脂質分子のボールによって表されます。 このような構造は、内部クリチンの姿勢という2つの相の分離に最適です。
リン脂質二球では、球状タンパク質が組み込まれており、その極性ジリアンが水相の親水性表面を踏みます。 タンパク質の統合 さまざまな機能、受容体、酵素、イオンチャネル、膜ポンプ、およびイオンと分子の担体を含みます。
活性タンパク質分子は脂質球の表面近くで自由に拡散します。 クリチン膜のさまざまな側面から現れるタンパク質分子の一部の元の状態では、それらの位置は変化しません。
膜の電気的特性:
電力の影響は主に、水和イオンを透過せず、同時に薄くする(約5 nm)リン脂質二重層によるものであるため、電荷の蓄積と陽イオンと陰イオンの静電相互作用は効果的ではありません。影響を受ける。 さらに、クリチン膜のパワーは、クリチン膜で実行される電気プロセスのクロック特性を決定する理由の1つです。
導電率(g)-電気的サポートを反転させ、イオンのグローバル膜貫通ストラムの値を、膜電位差を拡大した値に増加させる値。
異なるスピーチはリン脂質二重層、さらに浸透レベル(P)を介して拡散する可能性があるため、クリチン膜の構造によりスピーチの通過が可能になり、膜の側面に沿った拡散スピーチの濃度の違いになります。そして脂質膜の多様性と膜の力。
膜の導電率、世界、イオン透過性。 導電率の増加は、イオンが膜を通過するときのイオン数の増加を比較することです。
Budovaとイオンチャネルの機能。 それらはNa+、K +、Ca2 +、Cl-が細胞の中央に浸透し、特別な閉じたチャネルを通って入ります。 Rozmir kanalivdositmaly。
すべてのイオンチャネルは、次のグループに細分されます。
- 活気のある場合:
a)選択的に、次に。 明確な。 Qiチャネルは歌うイオンを貫通しています。
b)選択性が低く、非特異的で、歌うイオンの活気がある可能性があります。 Їх膜は少量です。
- スキップされるイオンの性質について:
a)カリウム
b)ナトリウム
c)カルシウム
d)塩素
- セキュリティを非アクティブ化するには、tobto。 カーリング:
a)非アクティブ化されている、つまり。 クロージングキャンプですぐに渡ります。 悪臭はMPの迅速な減少と同じ更新速度を処理します。
b)ひどく不活性化。 ЇkhnєvіdkrivannyavyklkaєMPのますます減少とますます多くのヨガの更新。
4.回復のメカニズムの背後にある:
a)潜在的な預金、つまり。 tі、膜の等しい電位でschovydkrivayutsya。
b)化学沈着物。これは、生理学的に活発な発話(神経伝達物質、ホルモンなど)が細胞膜の化学受容器に注入されたときに観察されます。
与えられた時間に、イオンチャネルがそのような生命を作ることができることが確立されました:
1.選択フィルター、女の子のチャンネルでステッチ。 Vіnは、厳密に歌うイオンがチャネルを通過することを保証します。
2.膜電位またはディップタイプPASと同じレベルで制御される活性化ゲート。 同じレベルのMPでそれらを開くセンサーを備えた電位沈着チャネルの活性化ゲート。
3.不活性化ゲート。これにより、チャネルが閉じられ、MPレベル(小)のチャネルを介してイオンによって固定されます。
非特異的イオンチャネルは干渉しません。
選択的イオンチャネルは、活性化(m)ゲートと不活性化(h)ゲートの位置に応じて、3か国で使用できます。
1.アクティブ化が閉じられ、非アクティブ化が閉じられている場合は閉じられます。
2.アクティブ化され、tіとіnshіgatevіdkritі。
3.非アクティブ化、アクティブ化ゲートが開いている、および非アクティブ化ゲートが閉じている
イオンチャネルの機能:
1.カリウム(穏やかな状態で)-穏やかな可能性の生成
2.ナトリウム-潜在的なdiyの生成
3.カルシウム-最も重要なものの生成
4.カリウム(ザトリマン矯正)-安全な再分極
5.カリウム-カルシウム活性化-脱分極の交換、Ca+2ストラムに囲まれている
イオンチャネルの機能 別の方法で。 電圧を固定する方法、つまり「電圧クランプ」を拡張してみましょう。 この方法の本質は、特別な電子システムの助けを借りて、プロセスが膜電位を同じレベルに変更および固定できることです。 これにより、膜を流れるイオン性ストラムの大きさが制御されます。 電位差がになっている場合、オームの法則によれば、ストリームの値はイオンチャネルの導電率に比例します。 脱分極の同じ段階で、電気化学的勾配に沿ってクリチンに入る他のチャネル、すなわち、クリチンを脱分極するイオン性ストラムがあります。 Qiaの変更は、keruyuchy podsiluvachの助けを借りて登録され、膜を通過します 電気ストラム、大きさに等しいが、膜イオン性ストラムの直線で増殖している。この場合、膜貫通電位差は変化しない。
「パスクランプ」電位をさらに局所的に固定するために、少数のチャネルの機能を改善することが可能です。 微小電極(マイクロピペット)を塩水噴霧で絞り、膜の表面に押し付けて小さな噴霧を作成します。 同時に、膜の一部が微小電極まで移動します。 ピックアップゾーンでイオンチャネルが検出されるとすぐに、単一チャネルのアクティビティが登録されます。 チャネルへの活動のいじめと登録のシステムは、電圧を固定するシステムの影響をほとんど受けません。
単一のイオンチャネルを通るストラムは長方形の形状をしており、さまざまなタイプのチャネルで同じ振幅を示します。 有効期限が切れる段階でのチャネルへのperebubovannyaの些細なことは、imovirnistnyの特徴かもしれませんが、膜電位の大きさに応じて横になります。 Sumarnyイオンストラムは、運河の歌唱量の特定の期間中の皮膚の内臓状態におけるその重要性によって特徴付けられます。
運河の外側は部分的にアクセス可能ですが、運河の内側は重要になります。 P. G. Kostyukは、微小電極をブロックすることなくイオンチャネルの入口および出口構造の機能を可能にする細胞内透析の方法を拡張するために使用されました。 喉のスペースの後ろで開いたイオンチャネルの一部は、その機能的な力のために、チャネルの一部で乾燥し、最も内側の中央でスタントしたように見えました。
イオンチャネル自体は、選択性と導電性という2つの重要な膜力を提供します。
チャネルへの選択性または活気は、その特別なタンパク質構造によって保証されます。 膜電位の大きさに応じて、これらの建物を堆積させることができるように、多数のチャネルが帯電しています。 チャネルは、その機能的特徴、特にチャネルへの入口とその出口(いわゆるcomirn_mechanisms)として知られているタンパク質構造の重要性に関して不均一です。
ナトリウムチャネルに関連するロボットチャネルの原理を見てみましょう。 ナトリウムチャネルが穏やかな状態で閉じられていることが重要です。 クリチン膜が最初のレベルに脱分極すると、m-活性化ゲート(活性化)が増加し、クリチンの中央でNa+イオンの摂取量が増加します。 m-voiceが聞こえてから数ミリ秒後、h-voritが閉じられ、ナトリウムチャネルが腐敗します(不活性化)。 脱分極刺激の大きさと時間に応じて、ゆっくりと横になる不活化の時間にもかかわらず、不活化はクリチン膜で発生します。
胸部神経線維に単一の電位diが生成されると、内部媒体中のNa +イオンの濃度は、巨大イカ軸索のNaイオンではなく、内部のタイプごとに1/1000000未満になります。
ナトリウムクリーム、クリチン膜には、他のタイプのチャネルが設置され、振動的に浸透するオクレミイオン:Do +、Ca2 +、およびこれらのイオンのさまざまなチャネルがあります。
ホジキンとハクスリーは、運河の「独立」の原則を策定しました。これは、膜を通るナトリウムとカリウムの流れが互いに独立していることを意味します。
異なるチャネルの導電率のパワーは同じではありません。 ゾクレマ、カリウムチャネルの場合、不活化のプロセスはナトリウムチャネルの場合と同じではありません。 Є内部の細胞カルシウム濃度が上昇し、細胞膜の脱分極が起こると活性化される特別なカリウムチャネル。 カリウム-カルシウム沈着チャネルの活性化は再分極を加速し、それによって穏やかな可能性の重要性を植え付けます。
特に興味深いのは、カルシウムチャネルを確立することです。 入口カルシウムストラムは、原則として、クリチン膜を通常脱分極させるのに十分な大きさではありません。 ほとんどの場合、彼女は二次的な仲介者として「メッセンジャー」の役割を果たします。 カルシウムチャネルの活性化は、例えばナトリウム入口流による細胞膜の脱分極によって確実になります。
カルシウムチャネルの不活性化のプロセスは折り畳み可能です。 片側から、遊離カルシウムの細胞内濃度を上げてカルシウムチャネルを不活性化します。 一方、細胞質タンパク質はカルシウムに結合します。これにより、低レベルではありますが、カルシウムストローマの安定した量を3回維持することができます。 このナトリウムストラムを使用すると、より敬意を払うようになります。 カルシウムチャネルは心臓細胞で重要な役割を果たします。 第7章の心筋細胞の電気発生。細胞膜の電気生理学的特性は、追加の特別な方法によってサポートされています。